Starlix diabetui gydyti
Prekės ženklas: Starlix
Bendrasis pavadinimas: nateglinido tabletės
Turinys:
apibūdinimas
Klinikinė farmakologija
Klinikiniai tyrimai
Indikacijos ir naudojimas
Kontraindikacijos
Atsargumo priemonės
Neigiamos reakcijos
Perdozavimas
Dozavimas ir administravimas
Kaip tiekiama
Starlix, nateglinidas, išsami informacija apie pacientą (paprasta angliškai)
apibūdinimas
Starlix® (nateglinidas) yra geriamasis diabetinis preparatas, naudojamas 2 tipo cukriniam diabetui gydyti [taip pat žinomas kaip nuo insulino nepriklausomas cukrinis diabetas (NIDDM) arba suaugusiųjų diabetas]. Starlix, (-) - N - [(trans-4-izopropilcikloheksanas) karbonil] -D-fenilalaninas yra struktūriškai nesusijęs su geriamaisiais sulfonilkarbamido grupės insulino sekreciją skatinančiais medžiagomis.
Struktūrinė formulė yra tokia, kaip parodyta
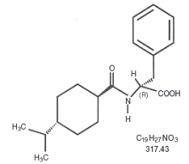
Nateglinidas yra balti milteliai, kurių molekulinė masė yra 317,43. Jis lengvai tirpsta metanolyje, etanolyje ir chloroforme, tirpsta eteryje, mažai tirpsta acetonitrilyje ir oktanolyje ir praktiškai netirpsta vandenyje. „Starlix“ abipus išgaubtoje tabletėje yra 60 mg arba 120 mg geriamojo nateglinido.
Neaktyvūs ingredientai: koloidinis silicio dioksidas, kroskarmeliozės natrio druska, hidroksipropilmetilceliuliozė, geležies oksidai (raudoni arba geltonasis), laktozės monohidratas, magnio stearatas, mikrokristalinė celiuliozė, polietilenglikolis, povidonas, talkas ir titanas dioksidas.
viršuje
Klinikinė farmakologija
Veiksmo mechanizmas
Nateglinidas yra aminorūgščių darinys, mažinantis gliukozės kiekį kraujyje, stimuliuodamas insulino sekreciją iš kasos. Šis veiksmas priklauso nuo veikiančių beta ląstelių kasos salelėse. Nateglinidas sąveikauja su ATP jautriu kalio (K + ATP) kanalu kasos beta ląstelėse. Vėlesnė beta ląstelės depoliarizacija atveria kalcio kanalą, sukuriant kalcio antplūdį ir insulino sekreciją. Insulino išsiskyrimo laipsnis priklauso nuo gliukozės ir mažėja esant žemai gliukozės koncentracijai. Nateglinidas yra labai selektyvus audiniams ir mažas giminingumas širdies ir griaučių raumenims.
Farmakokinetika
Absorbcija
Išgėrus prieš pat valgį, nateglinidas greitai absorbuojamas, o vidutinė didžiausia vaisto koncentracija plazmoje (Cmax) paprastai būna per 1 valandą (Tmax) po dozavimo. Kai skiriama pacientams, sergantiems 2 tipo cukriniu diabetu, nuo 60 mg iki 240 mg dozių diapazonas tris kartus per dieną vienai savaitę nateglinidas parodė tiesinę farmakokinetiką tiek AUC (plotas po laiko / plazmos koncentracijos kreive), tiek ir Cmax. Taip pat nustatyta, kad Tmax nepriklauso nuo dozės šioje pacientų grupėje. Apskaičiuota, kad absoliutus biologinis prieinamumas yra maždaug 73%. Išgėrus valgio ar po jo, nateglinido absorbcija (AUC) nepakinta. Vis dėlto absorbcijos greitis yra vėluojantis, pasižymintis Cmax sumažėjimu ir laiko, per kurį pasiekiama didžiausia koncentracija plazmoje (Tmax), vėlavimu. Kai nateglinidas vartojamas nevalgius, plazmos profiliams būdingos kelios koncentracijos plazmoje. Šis poveikis silpnėja, kai nateglinidas geriamas prieš valgį.
Paskirstymas
Remiantis duomenimis, gautais po intraveninio (IV) nateglinido vartojimo, nustatyta, kad sveikiems asmenims pastovus nateglinido pasiskirstymo tūris yra maždaug 10 litrų. Nateglinidas plačiai (98%) jungiasi su serumo baltymais, pirmiausia su serumo albuminais, ir mažesniu mastu Î ± 1 rūgšties glikoproteinu. Serumo baltymų prisijungimo laipsnis nepriklauso nuo vaisto koncentracijos bandymo intervale 0,1–10 µg / ml.
Metabolizmas
Prieš eliminaciją nateglinidas metabolizuojamas mišrių funkcijų oksidazės sistemos pagalba. Pagrindiniai metabolizmo keliai yra hidroksilinimas, po kurio vyksta konjugacija su gliukuronidu. Pagrindiniai metabolitai yra mažiau veiksmingi antidiabetiniai vaistai nei nateglinidas. Neesminis izopreno metabolitas turi tokią pat galią kaip pirminis junginys nateglinidas.
In vitro duomenys rodo, kad nateglinidą daugiausia metabolizuoja citochromo P450 izofermentai CYP2C9 (70%) ir CYP3A4 (30%).
Išsiskyrimas
Išgėrus, nateglinidas ir jo metabolitai greitai ir visiškai eliminuojami. Per 6 valandas po dozės suvartojimo maždaug 75% suvartoto 14C-nateglinido buvo išsiskyrusi su šlapimu. 85 proc. 14C-nateglinido buvo pašalinta su šlapimu, dar 10 proc. - su išmatomis. Maždaug 16% 14C-nateglinido išsiskyrė su šlapimu kaip pirminis junginys. Atliekant visus sveikų savanorių ir 2 tipo cukriniu diabetu sergančių pacientų tyrimus, nateglinido koncentracija plazmoje greitai sumažėjo, vidutinis pusinės eliminacijos laikas buvo maždaug 1,5 valandos. Atsižvelgiant į šį trumpą pusinės eliminacijos periodą, kartojant ne daugiau kaip 240 mg tris kartus per parą 7 dienas, nateglinido nesikaupė.
Vaistų sąveika
Vaistų metabolizmo tyrimai in vitro rodo, kad Starlix daugiausia metabolizuoja citochromo P450 izofermentas CYP2C9 (70%) ir mažesniu mastu CYP3A4 (30%). „Starlix“ yra galimas CYP2C9 izofermento inhibitorius in vivo, kaip rodo jo gebėjimas slopinti tolbutamido metabolizmą in vitro. In vitro eksperimentuose CYP3A4 metabolinių reakcijų slopinimo nenustatyta.
Glyburidas: randomizuotame kartotinių dozių kryžminio tyrimo tyrime pacientai, sergantys 2 tipo diabetu skiriama 120 mg Starlix tris kartus per dieną prieš valgį 1 dieną kartu su 10 gliburidu mg per parą. Kliniškai reikšmingų abiejų vaistų farmakokinetikos pokyčių nebuvo.
Metforminas. Kai Starlix 120 mg tris kartus per parą prieš valgį buvo skiriama kartu su metforminu 500 mg tris kartus Kartą per parą pacientams, sergantiems 2 tipo cukriniu diabetu, nei vieno, nei kito kliniškai reikšmingų farmakokinetikos pokyčių nebuvo agentas.
Digoksinas: Kai Starlix 120 mg prieš valgį buvo skiriama kartu su viena 1 mg doze Sveikiems savanoriams digoksino, nei vieno, nei kito kliniškai reikšmingo farmakokinetikos pokyčio nebuvo agentas.
Varfarinas: Kai sveikiems asmenims buvo skiriama 120 mg Starlix po tris kartus per dieną prieš valgį keturias dienas derinant su vienkartine 30 mg varfarino doze antrą dieną, nei vieno, nei kito farmakokinetika nepakito agentas. Protrombino laikas neturėjo įtakos.
Diklofenakas: skiriama 120 mg „Starlix“ ryto ir pietų dozė kartu su vienkartinėmis 75 mg dozėmis Sveikų savanorių diklofenako dozė reikšmingų farmakokinetikos pokyčių nepadarė agentas.
Specialiosios populiacijos
Geriatriniai: amžius neturėjo įtakos nateglinido farmakokinetinėms savybėms. Todėl senyviems pacientams dozės keisti nereikia.
Lytis: Kliniškai reikšmingų vyrų ir moterų nateglinido farmakokinetikos skirtumų nepastebėta. Todėl dozės koreguoti atsižvelgiant į lytį nereikia.
Rasė: Populiacijos farmakokinetinės analizės, įskaitant baltaodžių, juodaodžių ir kitos etninės kilmės asmenis, rezultatai rodo, kad rasė nedaro įtakos nateglinido farmakokinetikai.
Inkstų funkcijos sutrikimas: pacientai, sergantys 2 tipo cukriniu diabetu ir vidutinio sunkumo ir sunkus inkstų nepakankamumas (CrCl 15–50 ml / min), nesant dializės, parodytas panašus klirensas, AUC ir Cmax. Pacientams, sergantiems 2 tipo cukriniu diabetu ir inkstų nepakankamumu, atliekama dializė, bendras vaisto poveikis buvo mažesnis. Tačiau hemodializuojamų pacientų, palyginti su sveikų savanorių, jungimosi su plazmos baltymais sumažėjimas.
Kepenų funkcijos sutrikimas: Didžiausias ir bendras nateglinido ekspozicija nediabetais sergantiems asmenims, kuriems yra lengvas kepenų nepakankamumas, padidėjo 30%, palyginti su sveikų asmenų grupėmis. Starlix® (nateglinidą) reikia atsargiai vartoti pacientams, sergantiems lėtine kepenų liga. (Žr. ATSARGUMO PRIEMONĖS, Kepenų funkcijos sutrikimas.)
Farmakodinamika
„Starlix“ greitai absorbuojamas ir stimuliuoja kasos insulino sekreciją per 20 minučių po geriamojo vartojimo. Vartojant Starlix tris kartus per parą prieš valgį, greitai padidėja insulino kiekis plazmoje, didžiausia koncentracija kraujyje būna maždaug per valandą po dozavimo, o pradinė koncentracija sumažėja praėjus 4 valandoms po dozavimo.
Dvigubai aklame, kontroliuojamame klinikiniame tyrime, kuriame Starlix buvo skiriamas prieš kiekvieną iš trijų po valgio, gliukozės kiekis plazmoje buvo nustatytas per 12 valandų per parą po 7 savaičių gydymas. Starlix buvo vartojamas 10 minučių prieš valgį. Maistas buvo pagrįstas standartiniais diabeto svorio palaikymo meniu, nurodant bendrą kalorijų kiekį pagal kiekvieno tiriamojo ūgį. „Starlix“ sukelia statistiškai reikšmingą nevalgius ir po valgio glikemijos sumažėjimą, palyginti su placebu.
viršuje
Klinikiniai tyrimai
Devyniuose dvigubai koduotuose, placebu ar aktyviu būdu kontroliuojamuose 8–24 savaičių tyrimuose atsitiktinės atrankos būdu buvo įvertinti 3566 pacientai, siekiant įvertinti Starlix® (nateglinido) saugumą ir veiksmingumą. 3513 pacientų veiksmingumo vertės buvo didesnės nei pradinės. Šių tyrimų metu Starlix buvo vartojamas ne vėliau kaip 30 minučių prieš kiekvieną pagrindinį valgymą kasdien.
„Starlix®“ monoterapija, palyginti su placebu
Atsitiktinių imčių, dvigubai aklo, placebu kontroliuojamo 24 savaičių tyrimo metu 2 tipo diabetu sergantys pacientai, sergantys HbA1C, - 6,8 proc. tik dieta buvo atsitiktinai paskirta ir vartojant Starlix (60 mg arba 120 mg tris kartus per dieną prieš valgį) arba placebą. Pradinis HbA1C lygis svyravo nuo 7,9% iki 8,1%, o 77,8% pacientų anksčiau nebuvo gydomi geriamaisiais diabetais. Pacientai, kurie anksčiau buvo gydomi antidiabetiniais vaistais, turėjo atsisakyti šio vaisto vartojimo mažiausiai 2 mėnesius prieš atsitiktinę atranką. Įdėjus Starlix prieš valgį, statistiškai reikšmingai sumažėjo vidutinis HbA1C ir nevalgius nevalgius kraujo plazmoje (FPG), palyginti su placebu (žr. 1 lentelę). HbA1C ir FPG sumažėjimas buvo panašus pacientams, kurie anksčiau neturėjo vaistų nuo diabeto, ir tiems, kurie anksčiau buvo gydyti vaistais nuo diabeto.
Šiame tyrime pacientas, gydomas Starlix 120 mg tris kartus per parą prieš valgį, patyrė vieną sunkios hipoglikemijos epizodą (gliukozės kiekis plazmoje <36 mg / dL). Nei vienas pacientas nepatyrė hipoglikemijos, kuriai reikėjo trečiųjų šalių pagalbos. Starlix gydytų pacientų vidutinis kūno svorio padidėjimas, palyginti su placebu, buvo statistiškai reikšmingas (žr. 1 lentelę).
Kitame randomizuotame, dvigubai aklame, 24 savaičių, aktyviame ir placebu kontroliuojamame tyrime pacientai, sergantys 2 tipo cukriniu diabetu, buvo atsitiktinai suskirstyti į gydymą Starlix (120 mg tris kartus kasdien prieš valgį), 500 mg metformino (tris kartus per dieną), 120 mg Starlix (tris kartus per dieną prieš valgį) ir 500 mg metformino (tris kartus per dieną) deriniu, arba placebas. Pradinė HbA1C vertė svyravo nuo 8,3% iki 8,4%. Anksčiau penkiasdešimt septyni procentai pacientų nebuvo gydomi geriamaisiais diabetais. Monoterapija „Starlix“ sąlygojo reikšmingą vidutinio HbA1C ir FPG sumažėjimą, palyginti su placebu, kurie buvo panašūs į aukščiau aprašytų tyrimų rezultatus (žr. 2 lentelę).
1 lentelė: „Starlix®“ monoterapijos 24 savaičių fiksuotos dozės tyrimo baigties rezultatai
|
Placebas |
Starlix® 60 mg triskart kasdien prieš valgį |
Starlix® 120 mg triskart kasdien prieš valgį |
|
| HbA1C (%) | N = 168 | N = 167 | N = 168 |
| Pradinė vertė (vidurkis) | 8.0 | 7.9 | 8.1 |
| Pokytis nuo pradinio (vidutinis) | +0.2 | -0.3 | -0.5 |
| Skirtumas nuo placebo (vidutinis) | -0.5 a | -0.7 a | |
| FPG (mg / dL) | N = 172 | N = 171 | N = 169 |
| Pradinė vertė (vidurkis) | 167.9 | 161.0 | 166.5 |
| Pokytis nuo pradinio (vidutinis) | +9.1 | +0.4 | -4.5 |
| Skirtumas nuo placebo (vidutinis) | -8.7 a | -13.6 a | |
| Svoris (kg) | N = 170 | N = 169 | N = 166 |
| Pradinė vertė (vidurkis) | 85.8 | 83.7 | 86.3 |
| Pokytis nuo pradinio (vidutinis) | -0.7 | +0.3 | +0.9 |
| Skirtumas nuo placebo (vidutinis) | +1.0 a | +1.6 a |
p reikšmė â ‰ ¤ 0,004
„Starlix®“ monoterapija, palyginti su kitais geriamaisiais vaistais nuo diabeto
Glyburidas
24 savaičių, dvigubai aklu, aktyviu būdu kontroliuojamu tyrimu, kuriame dalyvavo 2 tipo cukriniu diabetu sergantys pacientai, kurie nuo 3 mėnesių vartojo sulfonilkarbamidą ir kurie turėjo pradinį HbA1C - 6,5% atsitiktinių imčių būdu buvo paskirta vartoti Starlix (60 mg arba 120 mg tris kartus per dieną prieš valgį) arba 10 mg gliburido. kasdien. Pacientams, atsitiktinai parinktiems į „Starlix“, reikšmingai padidėjo vidutinis HbA1C ir vidutinis FPG, palyginus su pacientais, atsitiktine tvarka parinktais į glicuridą.
Metforminas
Kitame randomizuotame, dvigubai aklame, 24 savaičių, aktyviame ir placebu kontroliuojamame tyrime pacientai, sergantys 2 tipo cukriniu diabetu, buvo atsitiktinai suskirstyti į gydymą Starlix (120 mg tris kartus kasdien prieš valgį), 500 mg metformino (tris kartus per dieną), 120 mg Starlix (tris kartus per dieną prieš valgį) ir 500 mg metformino (tris kartus per dieną) deriniu, arba placebas. Pradinė HbA1C vertė svyravo nuo 8,3% iki 8,4%. Anksčiau penkiasdešimt septyni procentai pacientų nebuvo gydomi geriamaisiais diabetais. Vidutinis HbA1C ir vidutinis FPG sumažėjimas, gavus monoterapiją metforminu, buvo žymiai didesnis nei šių kintamųjų sumažėjimas, vartojant monoterapiją Starlix (žr. 2 lentelę). Palyginti su placebu, Starlix monoterapija buvo susijusi su reikšmingu vidutinio svorio padidėjimu, tuo tarpu monoterapija metforminu buvo susijusi su reikšmingu vidutinio svorio sumažėjimu. Tarp pacientų, kurie nebuvo gydomi diabetu, pogrupyje vidutinis HbA1C ir vidutinis FPG sumažėjimas, vartojant monoterapiją Starlix, buvo panašūs kaip ir metformino monoterapijos metu (žr. 2 lentelę). Tarp pacientų, anksčiau gydytų kitais antidiabetiniais vaistais, pirmiausia gliburidu, HbA1C, pogrupyje „Starlix“ monoterapijos grupė šiek tiek padidėjo nuo pradinės, tuo tarpu HbA1C sumažėjo metformino monoterapijos grupėje (žr. 4 lentelę) 2).
„Starlix®“ kombinuota terapija
Metforminas
Kitame randomizuotame, dvigubai aklame, 24 savaičių, aktyviame ir placebu kontroliuojamame tyrime pacientai, sergantys 2 tipo cukriniu diabetu, buvo atsitiktinai suskirstyti į gydymą Starlix (120 mg tris kartus kasdien prieš valgį), 500 mg metformino (tris kartus per dieną), 120 mg Starlix (tris kartus per dieną prieš valgį) ir 500 mg metformino (tris kartus per dieną) deriniu, arba placebas. Pradinė HbA1C vertė svyravo nuo 8,3% iki 8,4%. Anksčiau penkiasdešimt septyni procentai pacientų nebuvo gydomi geriamaisiais diabetais. Pacientams, kurie anksčiau buvo gydomi antidiabetiniais vaistais, reikėjo nutraukti gydymą mažiausiai 2 mėnesiams iki atsitiktinės atrankos. Starlix ir metformino derinys statistiškai reikšmingai sumažino HbA1C ir FPG, palyginti su monoterapija Starlix ar metforminu (žr. 2 lentelę). „Starlix“ atskirai arba kartu su metforminu, palyginti su placebu ir metforminu, žymiai sumažino gliukozės koncentracijos padidėjimą prieš pradedant valgį iki 2 valandų po valgio.
Šiame tyrime buvo pranešta apie vieną sunkios hipoglikemijos epizodą (gliukozės kiekis plazmoje - 36 mg / dL), buvo pranešta apie Starlix ir metformino derinį ir keturis sunkios hipoglikemijos epizodus vienam pacientui, vartojusiam metforminą. gydymo ranka. Nė vienam pacientui nepatiko hipoglikemijos epizodas, dėl kurio reikėjo trečiųjų šalių pagalbos. Palyginti su placebu, „Starlix“ monoterapija buvo susijusi su statistiškai reikšmingu svorio padidėjimu, vartojant kartu su Starlix ir metforminu, reikšmingų svorio pokyčių nepastebėta (žr. 2 lentelę).
Į kitą 24 savaičių, dvigubai aklą, placebu kontroliuojamą tyrimą iš pradžių buvo įtraukti pacientai, sergantys 2 tipo cukriniu diabetu, sergantys HbA1C - 6,8% po gydymo metforminu (‰ 1500 mg per parą for 1 mėnesį). į keturių savaičių monoterapijos metforminu (2000 mg per parą) periodą ir atsitiktiniu būdu paskirstomas kartu su metforminu Starlix (60 mg arba 120 mg tris kartus per dieną prieš valgį) arba placebu. Kombinuotas gydymas Starlix ir metforminu buvo susijęs su statistiškai reikšmingai didesniu kraujo plazmos sumažėjimu HbA1C, palyginti su monoterapija metforminu (-0,4% ir -0,6% vartojant 60 mg Starlix ir 120 mg Starlix kartu su metforminu, atitinkamai).
2 lentelė: 24 savaičių Starlix® monoterapijos ir derinio su metforminu tyrimo baigties rezultatai
|
Placebas |
Starlix® 120 mg triskart kasdien prieš tai patiekalai |
Metforminas 500 mg triskart kasdien |
Starlix® 120 mg prieš tai maistas plius Metforminas * |
|
| HbA1C (%) | ||||
| Visi | N = 160 | N = 171 | N = 172 | N = 162 |
| Pradinė vertė (vidurkis) | 8.3 | 8.3 | 8.4 | 8.4 |
| Pokytis nuo pradinio (vidutinis) | +0.4 | -0.4 bc | -0.8 c | -1.5 |
| Skirtumas nuo placebo | -0.8 a | -1.2 a | -1.9 a | |
| NaÑ - ve | N = 98 | N = 99 | N = 98 | N = 81 |
| Pradinė vertė (vidurkis) | 8.2 | 8.1 | 8.3 | 8.2 |
| Pokytis nuo pradinio (vidutinis) | +0.3 | -0.7 c | -0.8 c | -1.6 |
| Skirtumas nuo placebo | -1.0 a | -1.1 a | -1.9 a | |
| Ne NaÑve | N = 62 | N = 72 | N = 74 | N = 81 |
| Pradinė vertė (vidurkis) | 8.3 | 8.5 | 8.7 | 8.7 |
| Pokytis nuo pradinio (vidutinis) | +0.6 | +0.004 bc | -0.8 c | -1.4 |
| Skirtumas nuo placebo | -0.6 a | -1.4 a | -2.0 a | |
| FPG (mg / dL) | ||||
| Visi | N = 166 | N = 173 | N = 174 | N = 167 |
| Pradinė vertė (vidurkis) | 194.0 | 196.5 | 196.0 | 197.7 |
| Pokytis nuo pradinio (vidutinis) | +8.0 | -13.1 bc | -30.0 c | -44.9 |
| Skirtumas nuo placebo | -21.1 a | -38.0 a | -52.9 a | |
| Svoris (kg) | ||||
| Visi | N = 160 | N = 169 | N = 169 | N = 160 |
| Pradinė vertė (vidurkis) | 85.0 | 85.0 | 86.0 | 87.4 |
| Pokytis nuo pradinio (vidutinis) | -0.4 | +0.9 bc | -0.1 | +0.2 |
| Skirtumas nuo placebo | +1.3 a | +0.3 | +0.6 |
p reikšmė â ‰ ¤ 0,05 vs. placebas
b p reikšmė â ‰ ¤ 0,03 vs. metformino
c p-reikšmė â ‰ ¤ 0,05 vs. derinys
* Metforminas buvo vartojamas tris kartus per parą
Rosiglitazonas
24 savaičių dvigubai aklas daugiacentris placebu kontroliuojamas tyrimas buvo atliekamas su 2 tipo pacientais diabetas, kurio terapinis atsakas į 8 mg rosiglitazono monoterapiją nėra tinkamai kontroliuojamas kasdien. Papildomas Starlix (120 mg tris kartus per dieną su maistu) vartojimas buvo susijęs su statistiškai reikšmingai didesniu HbA1C sumažėjimu, palyginti su monoterapija roziglitazonu. 24 savaičių skirtumas buvo –0,77%. Vidutinis svorio pokytis, palyginti su pradiniu, buvo maždaug +3 kg pacientų, gydytų Starlix ir rosiglitazonu, ir maždaug +1 kg pacientų, gydytų placebu ir rosiglitazonu.
Glyburidas
12 savaičių pacientų, sergančių 2 tipo cukriniu diabetu, nepakankamo gydymo 10 mg gliburidu kartą per parą tyrimo metu „Starlix“ (60 mg arba 120 mg tris kartus per parą prieš valgį) pridėjimas papildomo poveikio nedavė nauda.
viršuje
Indikacijos ir naudojimas
Starlix® (nateglinidas) skiriamas kaip priedas prie dietos ir mankštos, siekiant pagerinti glikemijos kontrolę suaugusiesiems, sergantiems 2 tipo cukriniu diabetu.
viršuje
Kontraindikacijos
Starlix® (nateglinidas) draudžiama vartoti pacientams, sergantiems:
1. Žinomas padidėjęs jautrumas vaistui ar jo neaktyviems ingredientams.
2. 1 tipo diabetas.
3. Diabetinė ketoacidozė. Šią būklę reikia gydyti insulinu.
viršuje
Atsargumo priemonės
Makrovaskuliniai padariniai: Klinikinių tyrimų, kuriuose būtų nustatyta įtikinamų makrovaskulinės rizikos sumažėjimo atvejų, vartojant „Starlix“ ar bet kurį kitą antidiabetinį vaistą, nebuvo.
Hipoglikemija: visi geriamieji sistemiškai absorbuojami gliukozės kiekį kraujyje mažinantys vaistai gali sukelti hipoglikemiją. Hipoglikemijos dažnis yra susijęs su diabeto sunkumu, glikemijos kontrolės lygiu ir kitomis paciento savybėmis. Vyresnio amžiaus pacientai, nepakankamai maitinami pacientai ir pacientai, kuriems yra antinksčių ar hipofizės nepakankamumas ar sunkus inkstų funkcijos sutrikimas, yra jautresni šių gydymo būdų gliukozės kiekį mažinančiam poveikiui. Hipoglikemijos riziką gali padidinti padidėjęs fizinis krūvis, alkoholio vartojimas, nepakankamas kalorijų kiekis ūminiu ar lėtiniu būdu arba derinimas su kitais geriamaisiais vaistais nuo diabeto agentai. Hipoglikemiją gali būti sunku atpažinti pacientams, sergantiems autonomine neuropatija ir (arba) tiems, kurie vartoja beta adrenoblokatorius. Starlix® (nateglinidas) turi būti vartojamas prieš valgį, kad sumažėtų hipoglikemijos rizika. Pacientai, kurie praleidžia maistą, taip pat turėtų praleisti numatytą Starlix dozę, kad sumažintų hipoglikemijos riziką.
Kepenų funkcijos sutrikimas: „Starlix“ reikia atsargiai skirti pacientams, sergantiems vidutinio sunkumo ar sunkia kepenų liga, nes tokie pacientai nebuvo tirti.
Glikemijos kontrolės praradimas
Dėl karščiavimo, infekcijos, traumos ar operacijos gali praeiti laikinas glikemijos kontrolės praradimas. Tokiais atvejais vietoje „Starlix“ gali prireikti gydymo insulinu. Gali atsirasti antrinis gedimas arba sumažėti „Starlix“ veiksmingumas tam tikrą laiką.
Informacija pacientams
Pacientus reikia informuoti apie galimą Starlix riziką ir naudą bei apie alternatyvius gydymo būdus. Turi būti paaiškinta hipoglikemijos rizika ir valdymas. Pacientams reikia patarti vartoti Starlix 1–30 minučių prieš valgant, tačiau praleisti numatytą dozę, jei jie praleidžia valgį, kad sumažėtų hipoglikemijos rizika. Vaistų sąveika turėtų būti aptarta su pacientais. Pacientai turėtų būti informuojami apie galimą vaistų sąveiką su Starlix.
Laboratoriniai tyrimai
Reakcija į gydymą turėtų būti periodiškai įvertinta atsižvelgiant į gliukozės kiekį ir HbA1C lygį.
Vaistų sąveika
Nateglinidas labai prisijungia prie plazmos baltymų (98%), daugiausia albumino. In vitro poslinkio tyrimai su labai prie baltymų prisijungusiais vaistais, tokiais kaip furosemidas, propranololis, kaptoprilis, nikardipinas, pravastatinas, gliburidas, varfarinas, fenitoinas, acetilsalicilo rūgštis, tolbutamidas ir metforminas nedarė jokios įtakos nateglinido baltymo kiekiui įrišimas. Nateglinidas taip pat neturėjo įtakos propranololio, gliburido, nikardipino, varfarino, fenitoino, acetilsalicilo rūgšties ir tolbutamido prisijungimui prie baltymų serume. Tačiau klinikinėje aplinkoje pagrįstas atskirų atvejų įvertinimas yra pagrįstas.
Tam tikri vaistai, įskaitant nesteroidinius priešuždegiminius vaistus (NVNU), salicilatus, monoaminooksidazės inhibitorius ir neselektyvūs beta adrenoblokatoriai gali sustiprinti „Starlix“ ir kitų geriamųjų vaistų nuo diabeto hipoglikeminį poveikį narkotikai.
Kai kurie vaistai, įskaitant tiazidus, kortikosteroidus, skydliaukės produktus ir simpatomimetikus, gali sumažinti „Starlix“ ir kitų geriamųjų vaistų nuo diabeto poveikį hipoglikeminiam poveikiui.
Kai šie vaistai skiriami pacientams, kuriems skiriama Starlix, ar jie nutraukiami, pacientą reikia atidžiai stebėti dėl glikemijos kontrolės pokyčių.
Vaistų ir maisto sąveika
Nateglinido farmakokinetikai įtakos neturėjo valgio sudėtis (daug baltymų, riebalų ar angliavandenių). Tačiau, kai Starlix buvo vartojamas 10 minučių prieš skystą maistą, didžiausia koncentracija plazmoje buvo žymiai mažesnė. Įvertinus acetaminofeno tyrimus, „Starlix“ neturėjo jokio poveikio sveikų asmenų skrandžio ištuštinimui.
Kancerogenezė / Mutagenezė / Vaisingumo pablogėjimas
Kancerogeniškumas: Dvejų metų kancerogeniškumo tyrimas su Sprague-Dawley žiurkėmis buvo atliekamas išgėrus nateglinido dozes iki 900 mg / kg per parą, kurios AUC žiurkių patinams ir patelėms, vartojantiems rekomenduojamą 120 mg Starlix dozę tris kartus per parą, atitinkamai maždaug 30 ir 40 kartų viršijančią terapinę žmogaus ekspoziciją. patiekalai. Dviejų metų kancerogeniškumo tyrimas su B6C3F1 pelėmis buvo atliktas išgėrus nateglinido dozes iki 400 mg / kg per parą, kurios AUC ekspozicija pasireiškė patinams Pelės ir patelės, maždaug 10 ir 30 kartų viršijančios terapinę žmogaus ekspoziciją, rekomenduojamos 120 mg Starlix dozės tris kartus per dieną prieš valgį. Nebuvo rasta nei tumorigeninio atsako nei žiurkėms, nei pelėms.
Mutagenezė: Nateglinidas nebuvo genotoksiškas atliekant in vitro Ames testą, pelės limfomos tyrimą, chromosomų aberacijos tyrimą Kinijos žiurkėno plaučių ląstelėse arba atliekant in vivo pelės mikronuklelio testą.
Vaisingumo pablogėjimas: Nateglinido vartojimas žiurkėms iki 600 mg / kg dozėmis nedarė įtakos vaisingumui. (maždaug 16 kartų didesnė už terapinę žmogaus ekspoziciją, prieš tai vartojant rekomenduojamą 120 mg „Starlix“ dozę tris kartus per parą patiekalai).
Nėštumas
C nėštumo kategorija
Nateglinidas nebuvo teratogeniškas žiurkėms, vartojusiems iki 1000 mg / kg dozes (maždaug 60 kartų viršijančios žmogaus terapinę ekspoziciją, vartojant rekomenduojamą 120 mg Starlix dozę tris kartus per parą prieš valgį). Triušio embriono raidai buvo padaryta neigiama įtaka, o tulžies pūslės agenezės ar mažo tulžies pūslės dažnis padidėjo. 500 mg / kg dozė (maždaug 40 kartų didesnė už terapinę žmogaus ekspoziciją su rekomenduojama 120 mg Starlix doze tris kartus per parą prieš patiekalai). Tinkamų ir gerai kontroliuojamų nėščių moterų tyrimų nėra. Starlix nėštumo metu vartoti negalima.
Darbas ir pristatymas
Starlix poveikis gimdymui ir gimdymui nėra žinomas.
Slaugos motinos
Tyrimai su žiurkėmis laktacijos metu parodė, kad nateglinidas patenka į pieną; piene ir plazmoje AUC0-48h santykis buvo maždaug 1: 4. Peri- ir postnataliniu laikotarpiu žiurkių, vartojusių 1000 mg / kg nateglinido, palikuonių kūno svoris buvo mažesnis. (maždaug 60 kartų didesnė už terapinę žmogaus ekspoziciją, prieš tai vartojant rekomenduojamą 120 mg „Starlix“ dozę, tris kartus per parą patiekalai). Nežinoma, ar Starlix patenka į motinos pieną. Kadangi daugelis vaistų išsiskiria į motinos pieną, Starlix neturėtų būti skiriama krūtimi maitinančiai moteriai.
Naudojimas vaikams
„Starlix“ saugumas ir veiksmingumas vaikams nenustatytas.
Geriatrinis vartojimas
Starlix saugumo ar veiksmingumo skirtumų tarp 65 metų ir vyresnių pacientų ir jaunesnių nei 65 metų pacientų grupėse nepastebėta. Tačiau negalima atmesti didesnio kai kurių vyresnio amžiaus asmenų jautrumo „Starlix“ terapijai.
viršuje
Neigiamos reakcijos
Klinikinių tyrimų metu maždaug 2 600 pacientų, sergančių 2 tipo cukriniu diabetu, buvo gydomi Starlix® (nateglinidu). Iš jų maždaug 1335 pacientai buvo gydomi 6 mėnesius ar ilgiau, o maždaug 190 pacientų - vienerius metus ar ilgiau.
Hipoglikemija buvo palyginti reta visose klinikinių tyrimų grupėse. Tik 0,3% Starlix pacientų gydymą nutraukė dėl hipoglikemijos. Virškinimo trakto simptomai, ypač viduriavimas ir pykinimas, nebuvo dažnesni pacientams, vartojantiems Starlix ir metformino derinį, nei pacientams, vartojantiems vien tik metforminą. Periferinė edema taip pat nebuvo dažnesnė pacientams, vartojusiems Starlix ir rosiglitazoną, nei pacientams, vartojantiems tik rosiglitazoną. Šioje lentelėje išvardyti įvykiai, kurie kontroliuojamų klinikinių tyrimų metu dažniau pasireiškė pacientams, vartojantiems Starlix nei placebą.
Dažni nepageidaujami reiškiniai (2% Starlix® pacientų) Starlix® monoterapijos tyrimuose (% pacientų)
| Placebas | Starlix® | |
| N = 458 | N = 1441 | |
| Pageidaujamas terminas | ||
| Viršutinė kvėpavimo takų infekcija | 8.1 | 10.5 |
| Nugaros skausmas | 3.7 | 4.0 |
| Gripo simptomai | 2.6 | 3.6 |
| Svaigulys | 2.2 | 3.6 |
| Artropatija | 2.2 | 3.3 |
| Viduriavimas | 3.1 | 3.2 |
| Atsitiktinė trauma | 1.7 | 2.9 |
| Bronchitas | 2.6 | 2.7 |
| Kosėjimas | 2.2 | 2.4 |
| Hipoglikemija | 0.4 | 2.4 |
Po pateikimo į rinką patirties buvo gauta retais padidėjusio jautrumo reakcijų, tokių kaip išbėrimas, niežėjimas ir dilgėlinė, atvejais. Panašiai buvo pranešta apie gelta, cholestazinį hepatitą ir padidėjusį kepenų fermentų kiekį.
Laboratoriniai anomalijos
Šlapimo rūgštis: Vidutinis šlapimo rūgšties kiekis padidėjo pacientams, gydomiems tik Starlix, Starlix kartu su metforminu, metforminu atskirai ir atskirai gliburidu. Atitinkami skirtumai nuo placebo buvo 0,29 mg / dL, 0,45 mg / dL, 0,28 mg / dL ir 0,19 mg / dL. Klinikinė šių išvadų reikšmė nežinoma.
viršuje
Perdozavimas
Klinikiniame tyrime, kuriame dalyvavo pacientai, sergantys 2 tipo cukriniu diabetu, buvo skiriama Starlix® (nateglinidas) didinant dozes iki 720 mg per parą 7 dienas, nebuvo jokių kliniškai reikšmingų nepageidaujamų reiškinių pranešė. Klinikinių tyrimų metu Starlix perdozavimo atvejų nebuvo. Tačiau perdozavus gali pasireikšti per didelis gliukozės kiekį mažinantis poveikis, atsirandant hipoglikemijos simptomams. Hipoglikemijos simptomai, neprarandant sąmonės ar nepatiriant neurologinių duomenų, turi būti gydomi geriama gliukoze ir koreguojant dozes ir (arba) valgant. Sunkias hipoglikemines reakcijas su koma, traukuliais ar kitais neurologiniais simptomais reikia gydyti į veną leidžiama gliukoze. Kadangi nateglinidas labai prisijungia prie baltymų, dializė nėra veiksminga priemonė jo pašalinimui iš kraujo.
viršuje
Dozavimas ir administravimas
Starlix® (nateglinidą) reikia vartoti 1–30 minučių prieš valgį.
Monoterapija ir derinimas su metforminu arba tiazolidindionu
Rekomenduojama pradinė ir palaikomoji Starlix dozė, vartojama atskirai arba kartu su metforminu arba tiazolidindionu, yra 120 mg tris kartus per parą prieš valgį.
60 mg Starlix dozė, atskirai arba kartu su metforminu ar tiazolidindionu, gali būti skiriama pacientams, kuriems gydymo pradžioje yra artimas HbA1C tikslas.
Dozavimas geriatrijos pacientams
Specialių dozių koreguoti nereikia. Tačiau negalima atmesti didesnio kai kurių asmenų jautrumo Starlix terapijai.
Dozavimas inkstų ir kepenų funkcijos sutrikimo atvejais
Pacientams, sergantiems lengvu ar sunkiu inkstų nepakankamumu ar lengvu kepenų nepakankamumu, dozės keisti nereikia. Dozavimas pacientams, kuriems yra vidutinio sunkumo ar sunkus kepenų funkcijos sutrikimas, nebuvo ištirtas. Todėl pacientams, sergantiems vidutinio sunkumo ar sunkia kepenų liga, Starlix reikia vartoti atsargiai (žr. ATSARGUMO PRIEMONĖS, Kepenų funkcijos sutrikimas).
viršuje
Kaip tiekiama
Starlix® (nateglinido) tabletės
60 mg
Rausva, apvali, nuožulniais kraštais tabletė, kurios vienoje pusėje yra įspaudas „Starlix“, o kitoje - „60“.
Buteliai po 100... NDC 0078-0351-05
120 mg
Geltona, ovalo formos tabletė, kurios vienoje pusėje yra įspaudas „Starlix“, o kitoje - „120“.
Buteliai po 100... NDC 0078-0352-05
Sandėliavimas
Laikyti 25 ºC (77 ºF) temperatūroje; leidžiama ekskursija iki 15 ºC-30 ºC (59 ºF – 86 ºF).
Išpilkite į sandarų indą, USP.
T2008-01
REV: 2008 M. LIEPOS mėn
Gamintojas:
„Novartis Pharma Stein AG“
Stein, Šveicarija
Paskirstė:
„Novartis Pharmaceuticals Corporation“
Rytų Hanoveris, Naujasis Džersis 07936
© „Novartis“
Paskutinį kartą atnaujinta 2008 07 07
Starlix, nateglinidas, išsami informacija apie pacientą (paprasta angliškai)
Išsami informacija apie diabeto požymius, simptomus, priežastis, gydymą
Šioje monografijoje pateikta informacija nėra skirta visoms galimoms naudojimo rūšims, nurodymams, atsargumo priemonėms, vaistų sąveikai ar neigiamam poveikiui. Ši informacija yra apibendrinta ir nėra skirta kaip specialūs medicinos patarimai. Jei turite klausimų apie vartojamus vaistus ar norite gauti daugiau informacijos, pasitarkite su gydytoju, vaistininku ar slaugytoja.
Atgal į: Naršykite visus vaistus nuo diabeto



